Nova determinação da Anvisa
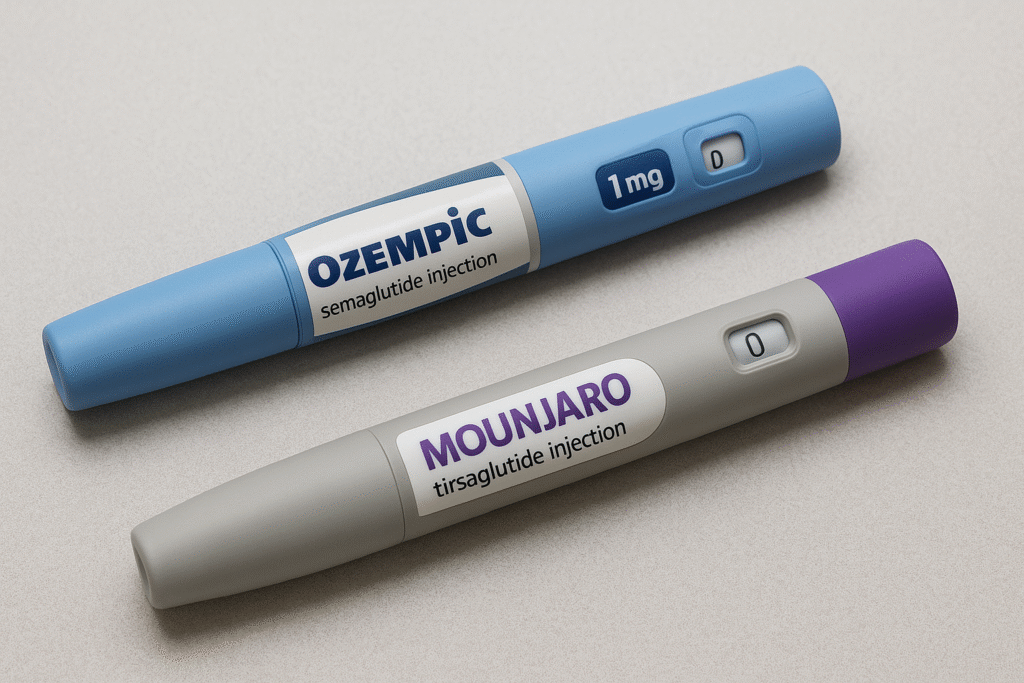
A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou uma importante mudança nas regras para a importação de Insumos Farmacêuticos Ativos (IFAs) utilizados em medicamentos injetáveis contra a obesidade no Brasil. Essa medida, divulgada na última segunda-feira, 25, tem como alvo específico as substâncias presentes em tratamentos populares como Ozempic e Mounjaro.
A decisão impacta diretamente as versões manipuladas desses medicamentos, que vinham sendo comercializadas no país sem a devida recomendação da Anvisa ou de entidades médicas. A agência destacou a necessidade de padronizar as normas de importação, especialmente no que diz respeito à liraglutida (Saxenda), semaglutida e tirzepatida, devido à complexidade e aos riscos sanitários associados à manipulação desses princípios ativos.
Impactos das novas regras
A Anvisa enfatizou que não basta garantir a qualidade e a efetividade dos insumos; é igualmente crucial assegurar a rastreabilidade de qualquer preparação derivada deles, incluindo as versões manipuladas em farmácias. Por isso, a agência determinou que somente empresas com registro na Anvisa estão autorizadas a importar os agonistas de GLP-1, substâncias utilizadas nas canetas para tratamento de obesidade e diabetes tipo 2.
A medida visa coibir a prática de manipulação inadequada, que tem levado ao uso de medicamentos de origem e pureza duvidosas. Clayton Macedo, diretor da Sociedade Brasileira de Endocrinologia e Metabologia (Sbem), ressalta que muitos pacientes têm recorrido a essas versões manipuladas, expondo-se a riscos devido à falta de garantias sobre a estabilidade e a eficácia dos produtos.
Reações do setor médico e farmacêutico
O endocrinologista Clayton Macedo alerta que, apesar do avanço representado pela nova medida, a vigilância da Anvisa deve ser ampliada para abranger de forma mais eficaz a tirzepatida, atualmente muito utilizada em manipulações. Ele aponta que a prática de vender e aplicar medicamentos antiobesidade em clínicas tem se tornado comum, o que fere o código de ética médica.
A farmacêutica dinamarquesa Novo Nordisk, responsável pela fabricação de Ozempic e Wegovy, manifestou apoio à decisão da Anvisa. Em nota, a empresa destacou que a determinação representa um avanço para a saúde pública, oferecendo maior segurança aos pacientes contra os riscos de produtos manipulados de forma inadequada. Medicamentos irregulares não garantem pureza, dosagem correta, estabilidade ou esterilidade, podendo resultar em tratamentos ineficazes e reações adversas graves.
Prioridade no registro de medicamentos
Em paralelo à nova regulamentação, a Anvisa informou que dará prioridade ao registro de medicamentos à base de liraglutida e semaglutida. Um edital foi lançado para permitir que as empresas solicitem análise prioritária, visando garantir o abastecimento desses medicamentos no Brasil.
Essa iniciativa surge após a área de fiscalização da Anvisa identificar instabilidade na oferta desses remédios no país. O balanço da agência revela que, até o início de setembro, foram realizados sete pedidos de registro de liraglutida e nove de formulações sintéticas de semaglutida. No setor de medicamentos biológicos, existem três processos em tramitação relacionados a esses insumos, ainda em fase inicial de análise técnica.
A decisão da Anvisa é um benefício para a saúde pública e para o paciente brasileiro, que passa a ter mais uma camada de proteção contra os riscos de produtos manipulados de forma ilegítima.
| Medicamento | Pedidos de Registro |
|---|---|
| Liraglutida | 7 |
| Semaglutida (sintética) | 9 |
Fonte: veja.abril.com.br
Veja Também:
- Estudo brasileiro indica que transplante de medula com doador meio compatível oferece mesma segurança que o de doador totalmente compatível
- Sete trilhas norte-americanas ideais para dar início às metas de condicionamento físico no Ano-Novo
- Cardiologist reveals why extreme fitness doesn’t always mean good health; stress may be the real culprit
- Raducanu desiste de duelo contra Osaka na United Cup e volta às quadras é adiada
- Problema no joelho coloca Taylor Fritz em dúvida para o Australian Open